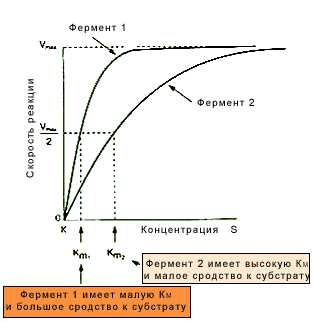
Активность фермента является одним из ключевых показателей его функциональности. Она представляет собой меру способности фермента к катализу реакций в организме. Влияние внешних факторов, таких как температура, pH-уровень и концентрация субстрата, оказывает непосредственное влияние на активность фермента.
Вопрос означает, каким образом ферментам удается так эффективно регулировать скорость химической реакции? Этот вопрос интересует не только ученых, но и студентов, изучающих химические науки. Несмотря на множество исследований по данной теме, механизмы, лежащие в основе активности ферментов, до конца не раскрыты.
Авторы этой статьи, Л.В. Боровская и С.Р. Гасе2, провели исследование, в котором было выявлено, что активность фермента зависит от концентрации ионов, а также состояния ионизации фермента и субстрата. Также, было установлено, что активные центры ферментов играют существенную роль в скорости реакций. Работы по этой теме были завершены с использованием теоретических знаний и экспериментальных данных, что позволило авторам достичь интересных результатов.
Взаимодействие фермента с субстратом и образование активного комплекса
Фермент-субстратное взаимодействие является количественным, то есть его интенсивность зависит от концентраций фермента и субстрата. Исследования в этой области позволяют установить оптимальные условия для реакции, а также выявить факторы, которые регулируют активность фермента. Например, научные работы с участием сфера регулирования активности ферментов могут включать примеры графиков, диаграмм или количественного анализа, чтобы проиллюстрировать зависимость между количеством субстрата и скоростью реакции.
Таким образом, фермент-субстратное взаимодействие и образование активного комплекса являются ключевыми процессами, которые определяют эффективность ферментативных реакций. Изучение этого физического механизма позволяет улучшить наши знания о функционировании фермента и выявить важные факторы, которые могут регулировать его активность. Научные исследования в этой области продолжаются, и результаты работы с учетом физических параметров могут иметь большое значение для различных областей наук и промышленности.
Влияние физических параметров на активность фермента
Физические параметры играют ключевую роль в регулировании активности ферментов, управляющих химическими реакциями в организмах. Авторы научных исследований посвятили значительное количество работ этому вопросу, их результаты имеют важное значение для наукам о жизни и промышленности. В данном разделе мы рассмотрим влияние физических факторов, таких как температура и pH, на активность ферментативных реакций.
Температура и ее роль в ферментативных реакциях
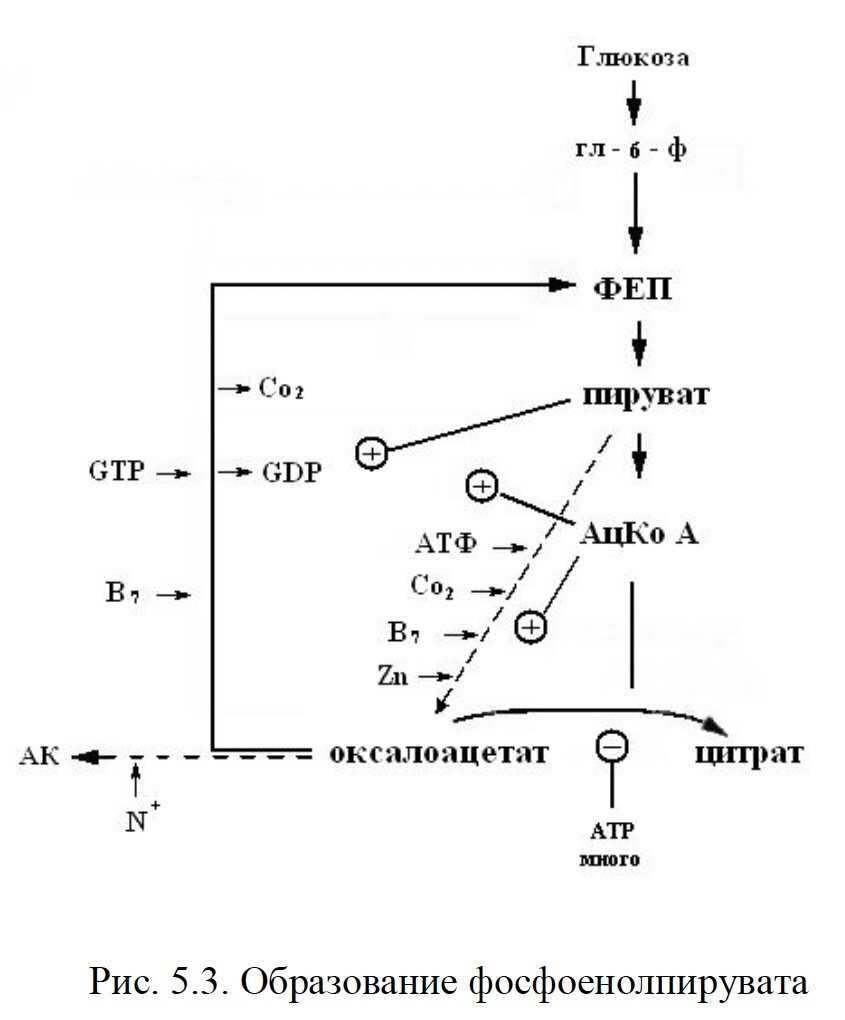
Одним из наиболее важных физических параметров, влияющих на активность ферментов, является температура. Она оказывает прямое влияние на скорость химических реакций, проводимых ферментами. Как было показано в исследованиях Барановой и Боровской, температура увеличивает активность фермента до определенного значения, после чего она начинает снижаться.
График зависимости скорости реакции от температуры может быть описан уравнением srgase2, где значения на оси ординат соответствуют активности фермента, а значения на оси абсцисс — температуре. Анализируя этот график, можно определить оптимальную температуру для проведения ферментативных реакций.
Влияние pH на кинетику ферментативных реакций
Еще одним важным фактором, регулирующим активность фермента, является pH-значение. Кислотность или щелочность среды, в которой происходят ферментативные реакции, существенно влияют на работу фермента. Наиболее чувствительны к изменениям pH ферменты, являющиеся активными в биологических системах.
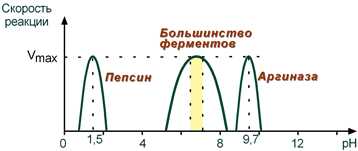
Исследования показывают, что каждый фермент имеет оптимальное pH-значение, при котором его активность достигает максимального значения. Более низкие или более высокие pH-значения оказывают негативное воздействие на активность фермента, что может привести к изменениям состояния его активного комплекса и, как результат, к снижению скорости реакции.
| Фактор | Влияние на активность фермента |
|---|---|
| Температура | Увеличение до оптимального значения, затем снижение |
| pH-значение | Оптимальное значение для каждого фермента |
Таким образом, физические параметры играют важнейшую роль в регуляции активности ферментов. Температура и pH-значение среды являются ключевыми факторами, влияющими на скорость ферментативных реакций. Понимание взаимосвязи между физическими условиями и активностью фермента имеет большое значение для улучшения эффективности биологических процессов и развития промышленности.
Влияние температуры на ферментативные реакции
Ферментативные реакции играют важную роль в биохимии и молекулярной биологии. Они позволяют ферментам катализировать химические реакции, ускоряя их и позволяя им происходить при относительно низких температурах.
Температура имеет прямое влияние на активность ферментов. При повышении температуры, реакции, участвующие в указанной процессе, происходят быстрее, и ферменты становятся более активными. Однако, слишком высокие температуры могут негативно влиять на структуру фермента и приводить к его денатурации.
Для каждого фермента существует оптимальная температура, при которой он проявляет максимальную активность. Например, фермент srgase2, который регулирует количественную зависимость активности от температуры, может иметь свою оптимальную температуру, с которой он осуществляет ферментативные реакции.
Факторы, влияющие на влияние температуры на ферментативные реакции:
- Структура фермента: каждый фермент имеет свою уникальную структуру, которая может определять, как он реагирует на изменения температуры.
- Тип химической реакции: различные типы реакций могут иметь разные температурные требования для эффективной катализации ферментом.
- Субстрат: свойства субстрата также могут влиять на взаимодействие с ферментом при разных температурах.
Боровская зависимость температуры на активность ферментов может быть описана количественным уравнением, которое отображает зависимость скорости реакции от температуры. Эта зависимость может иметь разную форму в зависимости от конкретного фермента и условий реакции.
Примеры влияния температуры на ферментативные реакции:
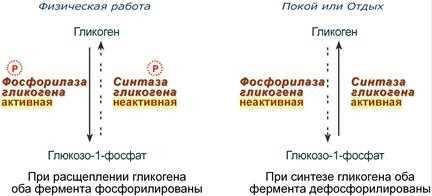
- Ферментативные реакции, участвующие в образовании и разрушении связей в молекулах глюкозы, имеют различные температурные оптимумы. Например, ферменты, отвечающие за образование гликозидных связей, обычно работают наиболее эффективно при температуре 37°C, что соответствует нормальной температуре человеческого организма.
- Фермент регулирующий процесс дыхания, работает наиболее эффективно при температуре около 25°C. При повышении или понижении температуры дыхательные процессы могут замедляться.
- Ферменты, участвующие в процессе синтеза белков, могут работать оптимально при разных температурах в зависимости от условий среды, в которой происходит реакция.
- Ферменты, связанные с пищеварением, могут иметь оптимальную температуру около 37°C, регулируя процессы расщепления пищевых веществ в желудочно-кишечном тракте.
Итак, влияние температуры на ферментативные реакции имеет значительное значение для эффективного функционирования фермента. Понимание этой зависимости позволяет биологам и химикам более глубоко исследовать ферменты и применять их в различных областях наук, включая медицину и пищевую промышленность.
Влияние pH на кинетику ферментативных реакций
В данной статье рассматривается важный аспект влияния pH на активность ферментов, являющийся одним из ключевых факторов контроля скорости ферментативных реакций. Изучение этого аспекта имеет большое значение как в научной, так и в прикладной области, поскольку позволяет более эффективно управлять ферментативными процессами в различных отраслях промышленности.
Значение pH для ферментов
Ферменты – это специфические белки, которые играют регуляторную роль в биохимических реакциях организма. Их активность зависит от ряда факторов, включая pH среды, в которой происходят реакции. Известно, что каждый фермент имеет оптимальный pH, при котором его активность будет наибольшей.
Ферменты отличаются по своей молекулярной структуре и уровню чувствительности к pH. Реакция, участвующая в процессе взаимодействия фермента с субстратом, зависит от электронного состояния фермента, которое в свою очередь определяется pH среды. Изменение pH может приводить к изменению различных химических свойств фермента, таких как ионизация аминокислот, структурные изменения и т. д.
Определение оптимального pH для фермента является важной задачей, так как это количественное значение позволяет оптимизировать условия ферментативных реакций. Различные ферменты имеют свои оптимальные значения pH, и исследование этих параметров становится основой для оптимизации кинетики и процессов синтеза в различных отраслях промышленности.
Взаимосвязь концентраций субстрата и активности фермента
Одной из важных особенностей влияния pH на ферментативные реакции является его взаимосвязь с концентрацией субстрата. Различные pH среды могут способствовать изменению эффективности взаимодействия между ферментом и субстратом. Изменение pH может приводить к изменению активности фермента, а следовательно, к изменению скорости и эффективности реакции.
Как следует из исследований, проведенных в данной области, pH среды оказывает значительное влияние на характер взаимодействия фермента с субстратом, а также на образование активного комплекса между ними. Различные значения pH могут способствовать ускорению или замедлению реакции, а также изменению направления ферментативного процесса.
Влияние внешних факторов на скорость ферментативных реакций
Работа многих научных специалистов в области ферментологии позволила выявить значительное влияние внешних факторов на скорость ферментативных реакций. Факторы, такие как внешняя температура, величина pH, концентрация субстрата и наличие ингибиторов, имеют важное значение для выполнения ферментами их активной роли в организме.
Особое внимание уделяется изучению влияния температуры на кинетику реакции, поскольку она играет существенную роль в скорости ферментативной активности. Л.В. Баранова и Е.И. Боровская, изучая ферментативную реакцию с фолиевой кислотой, заключили, что увеличение температуры способствует ускорению реакции, в то время как ее снижение приводит к замедлению. Однако выполнение реакции при высоких температурах может привести к денатурации фермента и потере его активности.
Кроме того, величина pH также оказывает значительное воздействие на скорость ферментативных реакций. Эксперименты показали, что каждый фермент имеет оптимальное значение pH, при котором он проявляет максимальную активность. Влияние pH на кинетику реакции обусловлено его ролью в поддержании оптимального состояния активного центра фермента и его субстрата.
Количество субстрата также играет важную роль в скорости ферментативных реакций. Увеличение его концентрации приводит к увеличению активности фермента, однако после достижения определенного значения, дальнейшее увеличение концентрации не оказывает значительного эффекта на скорость реакции.
Влияние внешних факторов на активность ферментов имеет важное значение для понимания принципов функционирования органической химии и биологических систем. Понимание этих факторов позволяет более глубоко и полно осуществлять исследования молекулярной активности ферментом, а также применять полученные знания для разработки новых методов и технологий в различных областях науки и будущей практике.
Научные и промышленные факторы, влияющие на скорость ферментативных реакций
Химические факторы

Один из основных химических факторов, влияющих на активность ферментов, — это сродство фермента к субстрату. Сродство характеризуется константой аффинности и определяет способность фермента связываться с субстратом и образовывать фермент-субстратный комплекс. Чем выше значение этой константы, тем эффективнее будет происходить реакция. Однако, внешние химические условия, такие как pH и концентрация ионов, могут снижать сродство фермента к субстрату.
Внешние факторы
Скорость ферментативных реакций также зависит от различных внешних факторов, таких как температура и pH. График скорости ферментативных реакций в зависимости от температуры отображает, что при низких значениях температуры скорость реакции значительно снижается. Однако, при повышении температуры, скорость реакции увеличивается, достигая своего максимума при определенной температуре, называемой оптимальной. Влияние pH также может оказывать значительное влияние на скорость ферментативных реакций. Каждый фермент имеет оптимальное значение pH, при котором он обеспечивает наивысшую активность. Изменение pH значительно снижает активность ферментов и может привести к полной потере их каталитической способности.
В общем, факторы, влияющие на скорость ферментативных реакций, являются сложной и важной темой, которая имеет применение как в научных исследованиях, так и в промышленности. Понимание этих факторов позволяет оптимизировать процессы и повысить эффективность использования ферментов для различных целей.

0 Комментариев